エビデンス
2020年末に新たな論文が通りました。画像で掲載いたします。
英語版のみですが、後日翻訳版が出ましたら追掲載いたします。
また、下記に解説を載せましたので併せてごらん下さい。





以下、解説
解説 4.演劇情動療法による認知症患者リハビリテーション医療の効率化
仙台富沢病院 前田有作、藤井昌彦、佐々木英忠
連絡先:佐々木英忠、982-0032 仙台市太白-区富沢字寺城11-4 仙台富沢病院、TEL:022-307-3375,FAX: 022-307-3376
Email: hsasakihide@yahoo.co.jp
Key Words: BPSD、antipsychotics, Neuropsychiatric Inventory、Delightful Emotional Index、dramatic performance
はじめに
医療は約30年ごとに変遷し感染症の時代に始まり、脳卒中、現在の癌、そして近未来の認知症の時代へと予想されている。認知症は90%以上の患者が行動・心理症状(Behavioral and Psychological Symptoms of Dementia, BPSD)を伴うと報告されており、BPSDは施設や認知症病院入院の原因となっている。BPSDのガイドライン (1) は最初に非薬物療法を施行し、効果が不十分な場合薬物療法を施行するとしている。非薬物療法は定期的なリハビリテーションであるが多くは効果が限られているため薬物療法を用いざるを得ない。薬物療法は抗認知症薬と向精神薬である。しかし、抗認知症薬はいずれも効果は少ない。向精神薬、中でも抗精神病薬はBPSDを抑制する力価が高いため効果があり処方されているが、副作用として高合併症率と死亡率が報告されている (2)。
抗精神病薬は本来統合失調症のため開発されてきた薬であり本来認知症には適応がない。日本では適応外処方として認可されている。50人もの認知症患者がいる病棟でシーンとしている場合があるが抗精神病薬による過鎮静の為であることが少なくない。抗精神病薬を含めた向精神薬は認知機能を抑制することが報告されている (3)。そうでなくとも物忘れしがちな脳に抗精神病薬を含めた向精神薬で抑制することは認知症の治療といえるのであろうか。認知症を早期発見しても認知症の助けになるという成績はない。抗認知症薬が認知機能(Mini-Mental State Examination, MMSE)(4)を1-2点くらい改善するから半年進行を遅らせると報告されているがMMSE1-2点改善は生活上影響がない。認知症への新しい取り組みが緊急の課題である。
Neuropsychiatric Inventory (NPI)
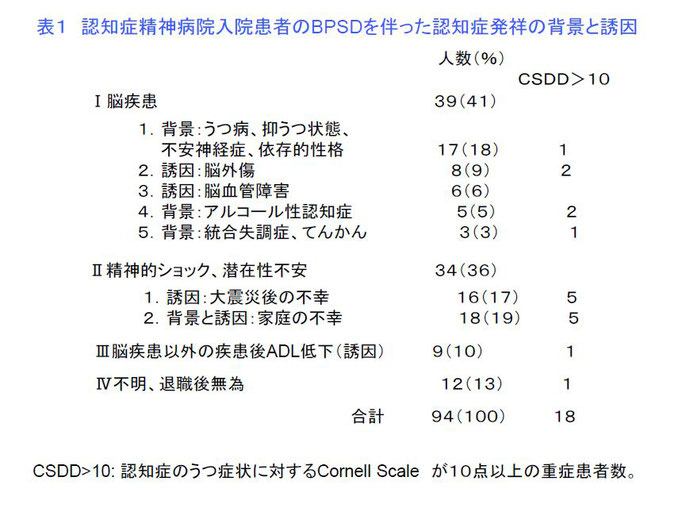
BPSDを評価する尺度はNPI (5)であるが NPIにはBPSDの暴力、暴言などの陽性症状からうつ症状、無反応などの陰性症状まで12項目を調査し0~108点までの点数で、低い点数ほどBPSDが少ないと判定する。BPSDがおおよそ30点以上で家族は疲弊し自宅あるいは施設から精神科認知症病院へ入院する例が多い。BPSDは約85%の人で何らかの不幸な出来事、生活環境あるいは家族関係(他人から見ると些細なことでも本人から見ると許せないことを含めて)などが誘引とみられ、ほとんどの人に苦悩があり、ある人は陽性症状になりある人は陰性症状になると思われる(表1) (6)。
入院後BPSDのガイドラインにのっとり定期的リハビリテーションを行うがほとんどのBPSDは改善せず向精神薬を処方することになる。BPSDの陽性症状があると介護が困難になり抗精神病薬を用いNPIを下げようとする。しかし、抗精神病薬を用いる人の中には無反応になり、時にはぐったりしよだれを流すなど過鎮静に至る場合が少なくない。このような状態は暴力などの陽性症状がなくなってNPIは低下し、介護しやすくなったので入院の目的は達成されたようにとらえられる。
しかし、NPIが低下したことは騒ぐことも暴力もなくなり介護者にとって介護しやすくなり助かるという状態になるが、反応がなくなることからあたかも人ではなく物を扱っているようになる。いくら働きかけても無表情で反応もないことから介護者はやりがいを感じなくなる恐れがある。やりがいがないということは仕事として面白さがなくなるということである。面白くなければ介護の仕事に就く人は減少する。加えて人ではなく物が対象なので誰でもできる仕事になり給料は安くなると悪循環に陥る。このようにNPIを目標にするBPSD治療には決定的な問題点が残ってしまう恐れがある (7)。そこで著者らは新しい観点からBPSDを治療することを試みた。
世間には誰かに喜びや笑いを誘うために私たちは何々をするという言葉であふれている。誰かに喜ばれることが最高の幸せなどである。認知症においても健常者と同様に喜びや笑いはあったほうが良いのではないか。特に抗精神病薬を用いてNPI を低下させた患者において反応がなくなることから喜びや笑いは少なくなるのではないかという危惧が残る。喜びや笑いを抜きにしてBPSDを治療することは許されるのであろうか。認知症のガイドラインには喜びや笑いについては触れられていない。そこで著者らは喜びや笑いの指標を作成した。
歓喜的情動指数(Delightful Emotional Index、DEI)
NPI の日本語訳はないが苦悩が上流にあるので仮にNPIは苦悩的情動指数といえると考えられる。著者らの勤務する精神科認知症病院である仙台富沢病院に入院中のBPSDの患者は入院当初陽性症状や陰性症状を表わすが、次第にBPSDが落ち着いてきて本来のやさしさが出てくるとNPIにはない喜びや笑いに近い情動を表すようになる。毎日の診療でNPI の指標とは相対する喜びや笑いにつながる指標を頻度の多い順に10項目にまとめ歓喜的情動指数(Delightful Emotional Index、DEI)を作成した (8)。
10項目は1:挨拶を返すことができる、2:表情がある、3:物事に関心を示す、4:話し合いをしようとする、5:喜ぶことができる、6:感謝することができる、7:賞賛に反応することができる、8:相手を気遣うことができる、9:ユーモアがある、10:善悪、美醜などを見分けることができる、である。各項目について程度(なし:0、少し:1、中程度:2、普通:3)X頻度(数日に1回:1、日に数回:2、常時:3)にて点数を付けた。満点は90点である。
精神科認知症治療病棟へ入院したBPSDの患者に無作為に抗精神病薬を処方した群と抗精神病薬以外の向精神薬を処方した群において6週後のDEIを比較した。BPSDの対象患者はアルツハイマー型認知症、脳血管性認知症、及びレビー小体型認知症でありそれ以外の診断の患者は除外した。向精神薬は調査の内容に関わっていない精神科医によって処方された。抗精神病薬を処方された抗精神病薬群(n=10)と抗精神病薬以外の向精神薬を処方された群(n=38)で比較調査した。ADLはBarthel Index (9)(0~100点で点数が高いほどADLが良い)、認知機能はMMSE(0~30点で点数が高いほど認知機能が良い), BPSDをNPI, 及び歓喜的情動をDEIで調査した。
入院時に両群のBarthel Index、MMSE,NPI,及びDEIに優位差はなかった。Barthel Index とMMSEは6週後入院時と変化はなかった。NPIは6週後には両群とも優位に低下した。しかし、抗精神病薬以外の向精神薬群では6週後のDEIは上昇したが、抗精神病薬群ではDEIは上昇せず、抗精神病薬以外の向精神薬群に比べて優位に低い値を示した(表2)。
上記の調査はBPSDのガイドラインに沿った治療であり両群ともNPIは低下し入院の目的は達成されている。しかし、その中にDEIが低下する群がありそれは抗精神病薬によってもたらされているようである。入院時のNPIは両群に差はなく抗精神病薬をBPSDの高い群に使用しているということではなかった。抗精神病薬を使用しない向精神薬の群ではDEIも上昇しているので好ましい治療になっているが、抗精神病薬を用いることによって喜びや笑いを持てる人間らしい生活ができなくなっていることを示唆しているのではないか。このことはNPIのみをBPSDの指標とする事は重大な欠点ではないかと考えられる。
BPSDをNPIの側から診ると、手っ取り早く効果の確かな抗精神病薬を用いてNPIを下げようとすることになってしまう傾向になると考えられるが、一方、DEIの側から診ると抗精神病薬を用いずにいかにNPIを下げることができるか更に工夫が必要になると考えられる。DEIを上げることによってNPIを下げるという視点はこれまで検討されておらず、全く新しい取り組みであると考えられる。
認知症は統合失調症と異なり高齢になるまで普通の生活をしてきた人であり、認知機能の低下によって勘違いの為苦悩的情動である陽性症状や陰性症状を出しているのであり本来のやさしさを持っている。統合失調症は突然症状が出て原因不明であるがBPSDには多くは気に障らないことをされたなどの理由があることが多い。BPSDさえなければいくら認知機能が低下してもご飯ですよ、お風呂ですよ、と言われ“ハイ”と言われるままに行動していれば在宅生活も可能になり、縁側に座って日向ぼっこをして過ごしていて隣近所のだれが訪ねてきたか忘れている単なるぼけ老人であり病院に連れて行って治療しなければならないということもなくなる。認知症の定義は認知機能の低下とともに社会生活ができなくなった状態とされており、BPSDがなく素直に在宅生活ができれば認知症の定義から外れる (10)。ここでBPSD成り立ちを再考してみたい。
新皮質と大脳辺縁系
認知機能劣化があるからBPSDが発生するので認知機能劣化が中核症状でBPSDは周辺症状と定義されてきたが果たしてそうであろうか。人の脳は永久に解らないと思われるが解っている範囲では認知機能を司る新皮質と情動を司る大脳辺縁系に分けられる。人は何かをしたいという情動(目的)に突き動かされて行動しようとする。情動を達成するために知識(新皮質)、体、道具を駆使する。エベレストに登りたいという情熱がある人はあらゆる困難を乗り越えて何とか達成しようとする。チンパンジーより人がすぐれている点は相手を思いやる気持ちを持つことであると報告されている (11)。情動が欠けている人はいくら認知機能が優れていても人間として欠けていることは自明の理である。
新入社員には知識がある人より情熱のある人が求められている。絶えず変遷する世において知識の豊富さを自認する人は自分の知識の範囲内で物事を解決しようとするため新しい問題に対応出来難い。それに対して情熱が高い人は何とか解決しようとあらゆる手段を用いて努力をするので解決の可能性が高い。人にとって情動(目的)を持つことが第一に必要であり知識は目的を達成するための道具の一つにすぎないので必要に応じて得られれば良い。大脳辺縁系(情動)が中核であり新皮質(知識)は末梢の一つであると考えられる (12)。
認知症にあてはめてみるとMMSEが低下しているので新皮質が劣化し末梢機能の低下があることには間違いないが、BPSDがあっても安心すると笑顔も見られるようになるなど情動機能が残っており大脳辺縁系の中核機能は比較的保たれているといえよう。認知機能の高低にかかわらずBPSDは発症する。いくら認知機能が低下してもBPSDがあるということは大脳辺縁系の情動機能は比較的保たれている事ではないかと考えられる。著者らはBPSDやDEIも含めた総合的情動機能検査としてMini-Emotional State Examination (MESE)を作成した (13)。図1は認知症のMESEのMMSEに対する分布を示している。MESEはMMSEにかかわらず比較的保たれMMSEが0点でもある程度の機能を持っていることが示された。
ニーチェは人の歓喜的情動は苦悩的情動よりはるかに深いと指摘している (14)。不幸な出来事は取り消すことができず苦悩的情動は残るが、一時でも歓喜的情動があれば人は前向きに生活できることから、認知症の治療はBPSDの低下のみならずDEIを上げることが目標であろう。従来BPSDの治療はNPIを下げることのみに目標をおいて治療してきたがDEIをも低下させる方法は治療とは言えないことになる。DEIを下げる抗精神病薬は認知症には極力使用すべきでないといえよう。実際、認知症治療病棟において抗精神病薬を全く使用しない例も報告されている (15)。
認知症治療病棟に入院してくる認知症では抗認知症薬は新皮質には少ししか刺激しないが大脳辺縁系を大いに刺激し少しの感情刺激にBPSDがますます増大する副作用が抗認知症薬使用例の約半数に見られる (16)。抗認知症薬によりBPSDが大きくなり、今度は抑制するために抗精神病薬を処方する例が少なからず見受けられ、あたかもアクセルとブレーキを同時に踏むような例で入院にいたる。抗精神病薬を含む向精神薬により認知症にさせられてしまう例など負の作用が報告されている (17)。
認知機能を保つには抗認知症薬や向精神薬を極力使用しないで、むしろ大脳辺縁系の中核症状である情動に心地よい刺激を加えることが二次的にBPSDを低下させると考えられる。大脳辺縁系の中核症状こそが認知症治療の目的ではないのか。精神科認知症病院へ入院する理由はBPSDでありMMSEの低下が理由の患者は皆無である。抹消症状をもたらす新皮質を非薬物療法で直接訓練しようとしても一時的で認知症には成功していない. 足腰、皮膚、感覚器、臓器などの道具である臓器の抗老化は個々では差があるものの全体としては成功していないと同様に認知機能も道具の一つであり抗老化は成功していない。百歳で百%認知症になることはやむを得ないと考えられる (18)。
認知症情動療法
DEIを上げる薬はない。抗精神病薬を使用しないことが第一であるが、更に積極的にDEIを上げるには非薬物療法で大脳辺縁系に良い刺激を与えるしかないと考えられる。認知症リハビリテーションとは身体のリハビリテーションも含まれるが多くは身体の老化が進み効率化は少ない。むしろ老化した知識や身体のような末梢機能を鍛えることではなく中核症状である大脳辺縁系の情動機能にいかに心地よい刺激を与えるかが最も必要なリハビリテーションと考えられる (19)。これまで行われてきた認知症リハビリテーションは運動療法、回想法、音楽療法、感覚刺激療法、アロマ療法 (20)、及び介護者の訓練されたマニュアルによる関わり方等々である。これらは認知機能やNPIの改善に効果があったことが報告され広く用いられている。しかし、DEIへの効果は不明である。
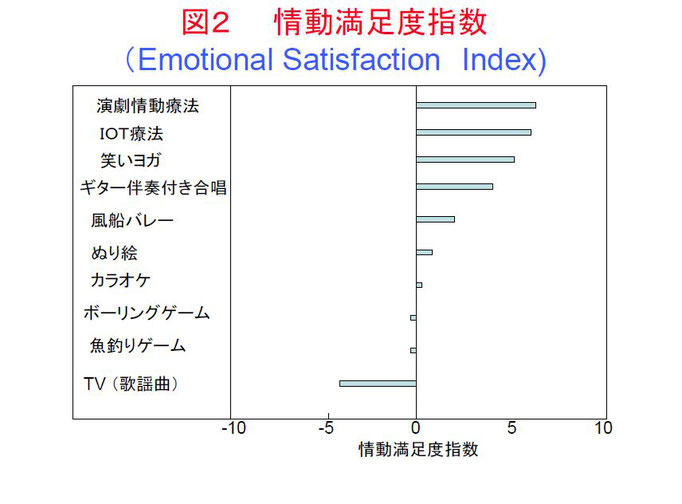
元気だった知人が認知症になり施設で幼稚な歌をみんなで歌っているのを見たくない、あるいは現在元気な自分が認知症といわれ施設で幼稚なリハビリテーションは受けたくないと考える人も少なくないと思われる。そこでリハビリテーション実行中にどのくらい参加者が満足しているのかを調査するため情動満足度指数(Emotional Satisfaction Index, ESI)を作成した (21)。ESIは実行中に参加者が目を覚ましている、興味ありそう、喜んでいる、など良い反応を5項目、眠っている、無視している、立ち去ろうとしている、など拒否的反応を5項目において0,1,2、点と強い反応順に点数をつけ、参加者全員の合計を参加人数で割り平均値を求める。10点が満点でー10点が最も低いESIである。対象はアルツハイマー型認知症、脳血管性認知症、レビー小体型認知症でMMSE>10におけるESIが図2である。精神科認知症病院で定期的に行われているリハビリテーションにはほとんど満足していなかった。満足しない弱い刺激で情動が刺激されることはないのは当然と考えられる。
認知機能がある程度保たれていて道理もある程度理解できる認知症患者は本人の情動嗜好にあった感動する情動刺激を繰り返し与えることによってDEIは高まりその結果NPIが低くなっていくのではないかと予想される (22)。しかし、人に感動させることは健常者でも相当の修行が必要である。まして認知症に感動を与えることはさらに困難と考えられる。医療・介護スタッフは不足し疲弊しているのが現状である。それでは外からの応援として芸術家の力を借りて感動する時間を持つことはDEIにどのような結果をもたらすのであろうか。
演劇情動療法(Dramatic emotional therapy, DET)
仙台富沢病院において8年前から演劇役者にボランティアをお願いして、週1回、1時間、10人位の認知症患者を対象に10分から40分感動するような物語(実話、小説、落語、など)をあたかも劇場で演劇を観ているように話して聞かせる演劇情動療法である (23)。対象は仙台富沢病院に入院したアルツハイマー型認知症、脳血管性認知症、レビー小体型認知症であり、MMSE>10点とした。入院前と入院後3カ月の成績を評価した。向精神薬は計画内容を知らされていない精神科医によって処方された。演劇情動療法介入群19名と非介入群26名が登録したが介入群では関心を示さなかった人や感染症などで不参加の人を除いて14名が、非介入群では感染症などの罹患者を除いて20名が完遂した。
患者は感動し感極まって泣いたりする。その後感想を述べ合う。戦中、戦後の経験、恋愛、家族のことなど話題が沸騰し笑いも出るようになる。参加者は次週を期待するようになった。表3は入院3か月前後の成績である。非介入群ではNPIは減少し、DEIは不変、向精神薬は薬剤間の力価が不明なので統計処理はできなかったが抗精神病薬は上昇傾向を示した。一方、介入群ではNPIは低下し、DEIは上昇、抗精神病薬は減少傾向を示した。非介入群は現在全国の認知症治療病棟で行われている実態であると考えられる。この状態に演劇情動療法を加えることでDEIが上昇しNPIは低下するという本来の治療といえる状態が得られている。
従来、回想療法など記憶を回復させる、又は、アロマ療法のような一時の心地よさなどが用いられてきたが人の機敏を味わうという試みは認知症には無理ではないかということで放置されてきたのではないか。しかし、認知症になっても感情は比較的健在で人としての感動を健常者と同様に感じる人たちが少なくないことが示された。演劇情動療法などを認知症リハビリテーション医療の効率化のため大いに取り入れる方向にかじを切るべきと思われる (24)。
物語を機械的に与えれば済むことではなく参加者をイメージして周到に選択され劇場にいるような本物の語り方によって場が劇場化すると考えられる。演劇役者は顔なじみになり、患者の機敏に触れる個々のキイワードを把握し対応することで安心感を与えることも苦悩的情動を一時的に忘れることにつながっていると考えられる。介入群で抗精神病薬が減る傾向にあることは、抗精神病薬による致死的疾病の頻度が多いことを考慮すると演劇情動療法のほうがはるかに医療費は安く健康的であると考えられる (25)。今後認知症リハビリテーション医療の効率化を上げるため社会的資源を活用する社会的処方箋を更に発展させなければならないと考えられる。
MMSEに無関係にDEIを上げる方法の一つはInternet of Things(IOT)療法である(26)。患者のキイワードに最もふさわしい動画をAIによりIOTのクラウドから引き出し患者の情動を刺激する方法である。全く無反応な患者に子供時代に過ごした街並みを動画で見せることによってじっと見入ったなどMMSEが低い人でも情動が動かされる。世界最高峰のオペラ歌手に思わず涙するなどである。IOT認知症リハビリテーションを週3回、一回20分行うことによりDEIは高まりNPIが低下した。この時一緒に診ている医療・介護者の優しさと的確な対応が必要である事はすべてのリハビリテーション医療に当てはまる。
道具である臓器医療はAI医療の時代になり手術を含めて医師の役割は減少すると考えられる (27)。医師の役割は人でなければできない情動療法に移行すると考えられる。情動療法の最大対象はBPSDで、BPSDにはリハビリテーション医療が主たる治療法である。ボランティアによる笑いヨガなども同様に社会的処方箋として有効である (28)。ボランティアが強制的に笑っているうちに参加者もつられて笑ってしまう療法である。BPSDに携わるすべての医療・介護職はAIが不得意とする情動療法を効率化することで必要とされる最先端の仕事になりやりがいも出て給料も上がると考えられる。今後量子情動療法など情動領域の発展が予想される(29)。
近未来医療費と介護費は対等になると予想されている。臓器医療・総合内科はAIが行い、老年内科・介護の目標は認知症も含めて老化した臓器医療・介護には限界があることから歓喜的情動をもたらすことであろう(図3)。情動療法がこれからの医療・介護の主流となると考えられる。
結語
本稿ではBPSDを中核症状と捉えることにより認知症の治療は従来のNPIを下げることからDEIを上げるという大きな認知症リハビリテーション医療が開け認知症は治療可能な疾患になったと考えられる。新皮質や身体の道具が劣化し例え寝たきりになってもBPSDがなく、ささやかな大脳辺縁系の喜び、即ち、孫が来てうれしい、介護者のちょっとした心使いがうれしいなど、新皮質の道具と大脳辺縁系の目的とが平衡がとれていれば(平行老化、Balanced Aging)QOLは高いといえよう (30)。演劇情動療法、IOT 療法、笑いヨガなどはDEIを上げる認知症リハビリテーション医療の効率化の例である。DEIを上げた先には平衡老化が認知症の治療目標である。
著者のCOI(Conflict of Interest)開示:本論文発表内容に関連して特に申告なし
文献
1. American Psychiatric Association Practice Guideline on the Use of Antipsychotics to Treat Agitation or Psychosis in Patients with Dementia. American Psychiatric Association Publishing. Washington, 2017.
2. Gill SS, Bronskill SE, Normand SL, et al. Antipsychotics drug use and mortality in older adults with dementia. Ann Intern Med 2007; 146: 775-786.
3. Azumi M, Ishizuka S, Fujii M, Sasaki H. Antipsychotics and cognitive function. Psychogeriatrics 2011; 11: 79-82.
4. Folstein MF, Folstein SE, Mc Hugh PR. “Mini-mental state”. A practical method for grading the cognitive state of patients for dementia. J Psychiatr Res 1975; 12: 189-198.
5. Cummings JL, Mega M, Gray K, et al. The neuropsychiatric inventory comprehensive assessment of psychopathology in dementia. Neurology 1994; 44: 2308-2314.
6. Hasegawa S, Tani K, Butler JP, et al. Backgrounds and/or triggers of hospitalized dementia with behavioral psychological symptoms. J Gerontol Geriatr Res 2017; 6; 2 DOI: 10.4172/2167-7182.100408.
7. 藤井昌彦、前田有作、金田理恵子、佐々木英忠。認知症情動療法。芳林社。東京都、2018.
8. Fujii M, Butler JP, Sasaki H. Antipsychotic drug use and favorable natures of emotional functions in patients with dementia. Psychogeriatrics 2019; 19: 320-324.
9. Mahoney FI, Barthel DW. Functional evaluation: the Barthel Index. Md State Med 1965; 14: 61-65.
10. 藤井昌彦、佐々木英忠。認知症は治療可能な疾患か?-BPSDの情動療法からみた考察。日本老年医学会誌 2017; 54: 114-118.
11. Myowa-Yamakoshi M, Scola C, Hirata S. Humans and chimpanzees attend differently to goal-directed actions. Nat Commun 2012; 3: 693. Doi: 10.1038/ ncomms 1695.
12. Fujii M, Butler JP, Sasaki H. Core symptoms and peripheral symptoms of dementia. Geriatr Gerontol Int 2018; 18: 979-980.
13. Fujii M, Butler JP, Hirazakura A, Sasaki H. Mini-Emotional State Examination for dementia patients. Geriatr Gerontol Int 2014; 14: 508-513.
14. Nietzsche F. Also sprach Zarathustra. Ein Buch für Alle und Keinen. Köln, 1883-1885.
15. Asanuma K, Sumi S, Fujii M, Sasaki H. Psychotropics for patients with dementia. Geriatr Gerontol Int 2013; 13: 1-2.
16. Fujii M, Sasaki H. Anti-dementia drugs in a psychiatric hospital for dementia patients. 2014; 14: 515-517.
17. 藤井昌彦、佐々木英忠。認知症情動療法によるポリファーマシー対策。老年内科 2020;1:183-192.
18. Ohrui T, Kubo H, Sasaki H. Care for older people. Intern Med 2003; 42: 932-940.
19. 藤井昌彦、佐々木英忠。量子情動療法と平行老化。老年内科 2020;1:16-20.
20. Fujii M, Hatakeyama R, Fukuoka Y, et al. Lavender aroma therapy for behavioral and psychological symptoms in dementia patients. Geriatr Gerontol Int 2008; 8: 136-138.
21. Maeda Y, Kaneda E, Fujii M, Sasaki H. Emotional Satisfaction Index for dementia patients. Geriatr Gerontol Int 2016; 16: 530-532.
22. Fujii M, Butler JP, Sasaki H. Emotional function in dementia patients. Psychogeriatrics 2014; 14: 202-209.
23. Maeda Y, Fukushima K, Kyoutani S, et al. Dramatic performance by a professional actor for the treatment of patients with behavioral and psychological symptoms of dementia. Tohoku J Exp Med 2020; 252: 263-267.
24. 藤井昌彦、佐々木英忠。演劇介護論による認知症介護。日本老年医学会誌 2018; 55: 686-690.
25. Butler JP, Fujii M, Sasaki H. New lessons of nurturing life for geriatric patients. Tohoku J Exp Med 2012; 227: 203-210.
26. Fukushima K, Aita E, Butler JP, et al. Emotional therapy using internet of things for behavioral and psychological symptoms of dementia. Geriatr Gerontol Int 2020; 20: 502-503.
27. Frey VB, Osborne MA. The future of employment: How susceptible are jobs to computerization? 2013; Oxford University Press.
28. 羽根田潔、佐藤四郎、恵美美紀、ほか。認知症行動・心理症状に対する笑いヨガの効果。日本認知症ケア学会誌 (印刷中)。
29. Fujii M, Ponsillo N, Boot J, et al. Hypothesis of quantum emotional therapy for behavioral and psychological symptoms of dementia. J Alzheimers Neurodegener Dis 2020; 6: 039 DOI: 10.24966/AND -9608/100039.
30. Butler JP, Fujii M, Sasaki H. Balanced aging, or successful aging? Geriatr Gerontol Int 2011; 11: 1-2.
図の説明
図1:認知機能(MMSE)と情動機能(MESE)の関係。
図2:各種のリハビリテーションに対する情動満足度指数(ESI)。文献21より改変。
図3:臓器医療・総合内科は主にAIが行い(実線)、老年医療は介護と連携して限界のある臓器医療や身体介護より喜びをもたらす情動療法に目標を置くようになる(点線)。

演劇情動療法を3ヶ月間受けた認知症患者のMESEとMMSEの数値の変化。演劇情動療法により認知機能(MMSE)は不変であったが情動機能(MESE)は改善した。

情動満足度指数(ESI)はプログラムによりばらつきがある。最もESI値が高いのが演劇情動療法である。
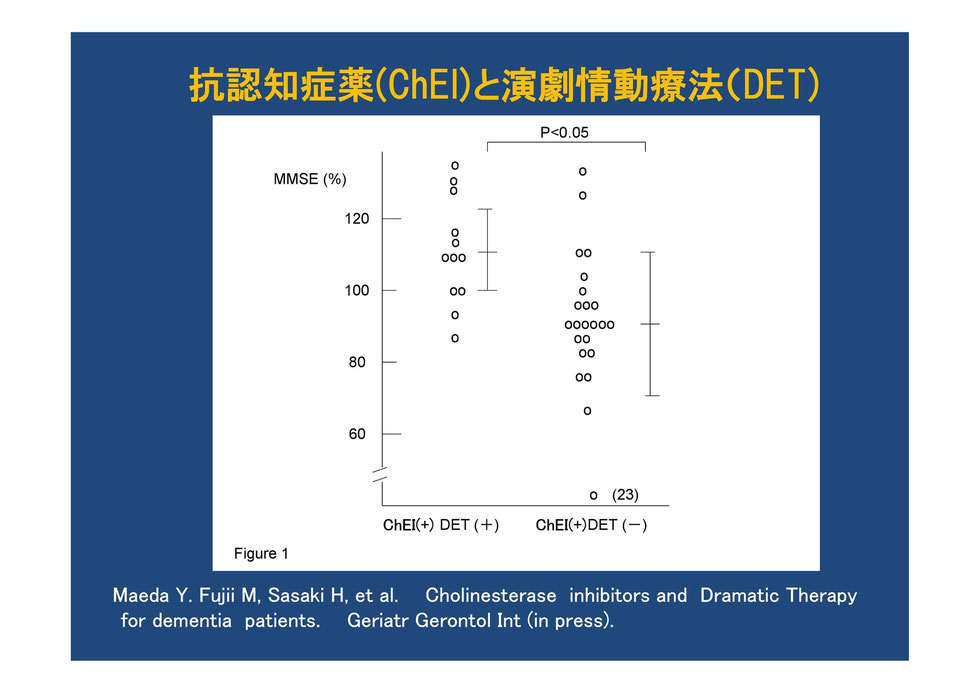
コリン分解酵素阻害薬を使用しても長期間のうちにMMSEの数値が下がるが、演劇情動療法を加えるとMMSEの数値は保たれている。

NPI(Neuropsychiatric Inventory) :認知症で問題となるBPSD(介護抵抗や徘徊などの行動・心理症状)の度合いを示す。
DEI (Deraitful Emotion Index) :笑う、喜ぶ、感動する、気遣いができる、などの歓喜的情動が残っている度合いを示す。
抗精神病薬:BPSDを抑えるために処方される薬。
一般的にBPSDを抑えるために抗精神病薬を用いるが、時間が経つに従い処方箋の数を増やさねばならない。しかし一方で、認知症当事者は薬の効果により人としての喜びを感じることができなくなり、歓喜的情動指数が下がってしまう。演劇情動療法を行った群では、NPIを下げつつ抗精神病薬を減らしている。
演劇情動療法によって歓喜的情動が増えることでBPSDが落ち着き、薬の使用も減らすことができた。